Cuando la medicina se olvida de las mujeres
En el siglo pasado, a finales de los años cincuenta y principios de los sesenta, tuvo lugar el que fue probablemente el primer desastre farmacológico a gran escala de la historia moderna, un evento que condicionó seriamente la salud femenina y cuyas consecuencias colean hasta el día de hoy. Se trata del caso de la talidomida, un medicamento que se comercializó en muchos países y que fue recetado a mujeres embarazadas para aliviar las náuseas y los vómitos, pero del que no había suficientes estudios sobre su seguridad. Como resultado, más de 10.000 niños y niñas de 46 países diferentes nacieron con graves malformaciones, problemas cardíacos, renales, auditivos… Aquella negligencia tuvo un gran impacto en la forma en la que se diseñaban los ensayos clínicos y, en particular, en la exclusión de mujeres en edad fértil, especialmente aquellas que estaban gestando.
Una exclusión histórica
Antes de aquel suceso, la presencia de la mujer en los ensayos clínicos también era mínima. Esto era debido a la aplicación, por norma, de la “medicina bikini”, un término acuñado para criticar el enfoque que históricamente la medicina daba a la salud femenina, centrándose únicamente en los órganos reproductivos e ignorando el sistema cardiovascular, neurológico, las enfermedades mentales o musculoesqueléticas, entre otras patologías. Pero a raíz del escándalo, aquella discreta ratio empeoró aún más, porque organismos como la Administración de Alimentos y Medicamentos estadounidense (FDA, por sus siglas en inglés) impusieron nuevas directrices que excluían a las mujeres en edad fértil de los ensayos clínicos.
Desde entonces, las mujeres fueron sistemáticamente apartadas de la investigación médica, incluso de estudios no relacionados con el embarazo; también de otras enfermedades y fármacos para tratarlas, creando un vacío de datos sobre eficacia y seguridad de medicamentos en la mitad de la población. Este hecho, que pretendía evitar casos como el de la talidomida, iba a comprometer la salud femenina durante las próximas décadas.
Dosis superiores y más efectos adversos
Las consecuencias de la falta de representación femenina en los ensayos clínicos son claras. En muchos casos, las mujeres reciben dosis más elevadas de las que realmente necesitan y esto deriva en un mayor riesgo de experimentar reacciones adversas. Esto se debe a que no se tuvieron en cuenta diferencias biológicas relevantes en el ensayo, como la actividad de ciertas enzimas en el organismo femenino (por ejemplo, en el hígado al metabolizar los fármacos) o la forma en que los riñones eliminan las sustancias de desecho (con una capacidad de filtración generalmente mayor en los hombres).
Según el Consejo General de Colegios de Farmacéuticos, hay numerosos medicamentos de uso habitual en los que sería necesario ajustar la dosis. Es el caso de las estatinas –que en mujeres aumentan el riesgo de mialgias y diabetes– o los antibióticos, ya que algunos órganos femeninos tienen más dificultades para eliminarlos. También sucede con las benzodiacepinas, los antihistamínicos y los antipsicóticos, los betabloqueantes, el hierro, la aspirina o ciertos tratamientos para la insuficiencia cardiaca, como la digoxina. Las mujeres presentan mayor riesgo de somnolencia con los antihistamínicos; metabolizan más despacio los betabloqueantes; absorben el hierro en mayor proporción que los hombres y necesitan dosis más bajas de los fármacos empleados para tratar la hipertensión arterial y otras enfermedades cardiovasculares como la insuficiencia cardiaca.
Cambios en la regulación
Muchas enfermedades que afectan especialmente a mujeres, como ciertas cardiopatías o el lupus, o incluso las condiciones hormonales, quedaron mucho menos estudiadas, algo que todavía afecta a la práctica médica de hoy. A pesar de que a finales de los ochenta y principios de los noventa la FDA decidió levantar el veto a las mujeres fértiles en los ensayos clínicos, todavía queda muchísimo por hacer. 30 años después, las mujeres aún no están representadas al nivel que se debería. Algunos informes de la FDA hablan de un 43% (incluyendo todas las fases de los ensayos), pero un estudio elaborado por la Universidad de St John’s en Nueva York cifra su participación en la primera fase de los ensayos clínicos, en los que se comprueba la seguridad, en un 21%.
Alberto M. Borobia Pérez, especialista de la Sociedad Española de Farmacología Clínica (SEFC) y médico del Hospital Universitario La Paz de Madrid, se encuentra en la actualidad inmerso en el Proyecto READI (Research in Europe and Diversity Inclusion), una iniciativa europea que tiene como objetivo cambiar la manera en la que se hacen los ensayos clínicos. “Claramente ha cambiado el panorama desde los noventa y desde la Comisión Europea se está trabajando en que esto suponga un cambio de paradigma en la manera en la que se diseñan y desarrollan los ensayos clínicos. Un ejemplo de ello es el Proyecto READI (1 y 2), en el que trabajamos para cambiar la manera en la que se realizan los ensayos, desde la fase de diseño hasta su desarrollo, con medidas que permitan mejorar la inclusión de poblaciones infrarrepresentadas en Europa”, señala Borobia.
Desde hace unos años se han establecido protocolos de seguridad, que antes no existían. Se evalúa desde las primera fase del ensayo si el fármaco en cuestión puede usarse en embarazadas, el riesgo-beneficio de incluirlas y, además, se ha marcado un protocolo por si la mujer participante se queda embarazada durante el transcurso del ensayo. En este caso prevalece el valor científico y no supone automáticamente su expulsión de la investigación.
Las consecuencias del retraso
Sin embargo, décadas sin la participación de las mujeres en los ensayos clínicos han tenido consecuencias. “Existen factores que explican qué le pasa al fármaco en el cuerpo y viceversa que difieren entre sexo masculino y femenino, por lo que una baja representación de mujeres en el desarrollo de un medicamento puede conllevar que la evidencia que se ha generado no sea aplicable a toda la población”, matiza el especialista. Este sesgo en la ciencia ha tenido consecuencias a la hora de diagnosticar y tratar enfermedades como el párkinson.
Un reciente trabajo llevado a cabo por investigadores del University College de Londres (UCL), la Escuela de Medicina de Harvard y el Hospital General de Massachusetts analizó datos de más de 10.000 personas con párkinson y encontró diferencias importantes en la manera que la enfermedad se presenta, evoluciona y responde terapéuticamente según el sexo del paciente. El informe destaca que los hombres reciben antes el diagnóstico porque las mujeres tienden a presentar síntomas distintos, incluyendo una mayor prevalencia de depresión, ansiedad y trastornos del sueño.
“En la consulta del especialista estas diferencias no se comprenden completamente debido a la escasez de datos por sexo provenientes de grandes estudios clínicos. Además, las mujeres pueden experimentar trayectorias distintas en la progresión de la enfermedad y en la respuesta a tratamientos como la estimulación cerebral profunda, las terapias sintomáticas aprobadas o los tratamientos con dispositivos médicos”, señalan las responsables de este trabajo. En concreto con el párkinson, los científicos se han planteado la hipótesis de que hormonas como los estrógenos podrían tener efectos neuroprotectores, que influyen en el riesgo y en la progresión de la enfermedad, pero los mecanismos y la relevancia clínica de estas influencias hormonales aún no están suficientemente estudiados por no contar con la suficiente representación de mujeres.
En la actualidad existen distintas barreras que dificultan la participación en algunos ensayos clínicos, que afectan a hombres y mujeres, como la falta de tiempo o de recursos para desplazarse –especialmente desde zonas rurales– o el limitado acceso a la información sobre el estudio, entre otras. A esto se suman ciertos mitos que generan desconfianza.
- Qué es un ensayo clínico. Son estudios de investigación médica cuyo objetivo es evaluar nuevas alternativas terapéuticas que han mostrado resultados prometedores en el laboratorio, con el fin de comprobar su eficacia y seguridad.
- ¿Por qué es necesaria una participación amplia? Para avanzar en el conocimiento de las enfermedades y en el desarrollo de tratamientos, es imprescindible contar con información más completa y analizar poblaciones diversas, incluyendo a minorías raciales y étnicas que suelen estar infrarrepresentadas.
- ¿Cómo podemos saber si un ensayo es adecuado para nosotros? En ocasiones es el propio médico que atiende al paciente quien informa de la existencia de un ensayo apropiado. Si sabemos de alguno que nos interesa, lo más recomendable es consultarlo siempre con el profesional sanitario.
- ¿Son seguros? Los ensayos clínicos son evaluados por un Comité de Ética y por las Autoridades Sanitarias, que revisan su validez y garantizan que se cumpla el protocolo, así como que el paciente reciba toda la información necesaria.
¿Por qué las mujeres participan menos?
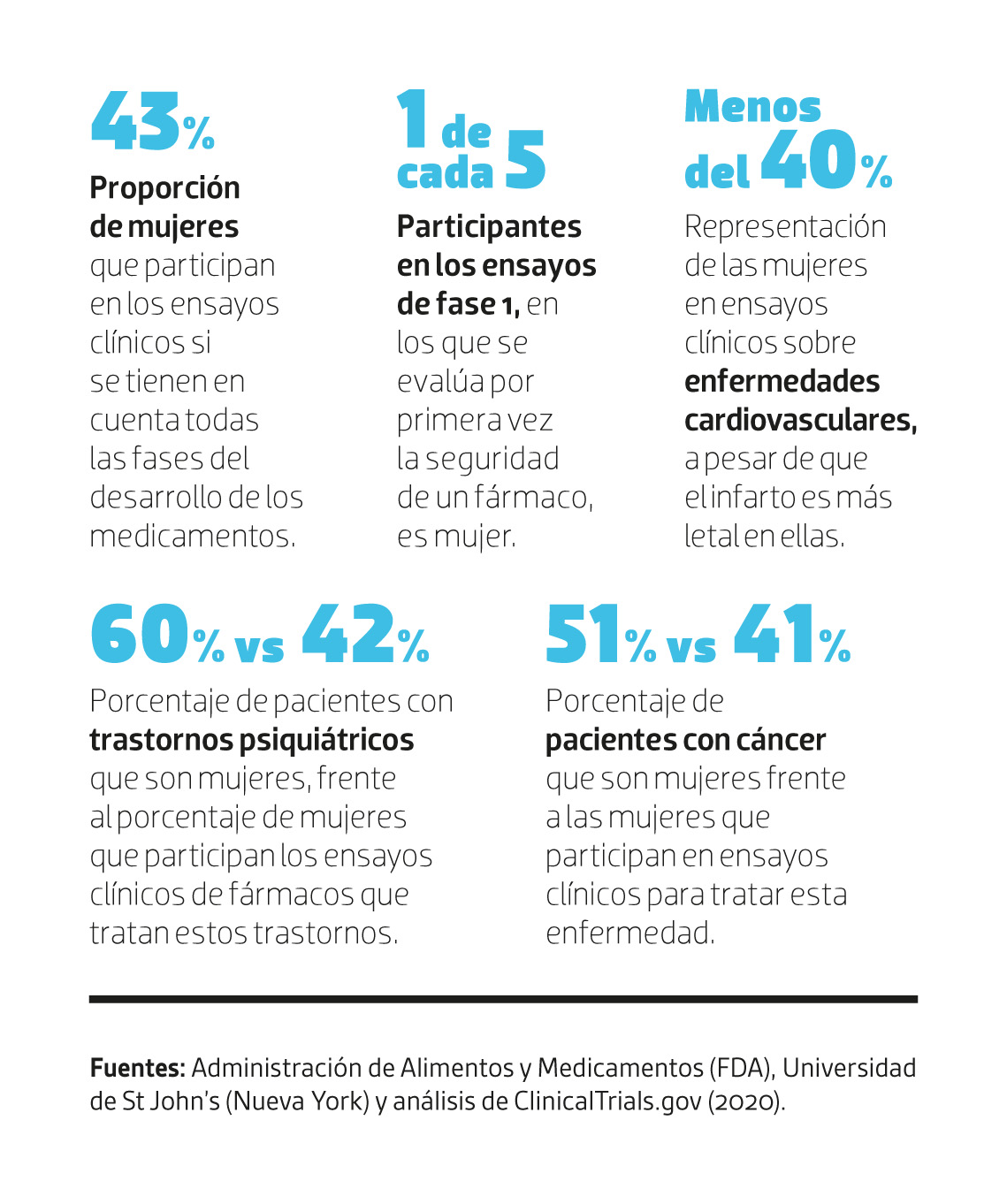
Las enfermedades cardiovasculares son la principal causa de muerte a nivel mundial, tanto en hombres como en mujeres. Sin embargo, y a pesar de que un infarto es más letal en ellas (menos tasa de supervivencia), siguen estando subrepresentadas en las investigaciones que definen la atención clínica. Por ejemplo, un análisis de 2020 de datos de ClinicalTrials.gov, la plataforma online en la que están colgados todos los ensayos clínicos que se están llevando a cabo en el mundo, encontró que las mujeres representaban menos del 40% de los participantes en estudios sobre enfermedades cardíacas y accidentes cerebrovasculares. Esta subrepresentación abarca múltiples áreas: las mujeres representan el 42% de los participantes en ensayos sobre trastornos psiquiátricos, aunque constituyen el 60% de los pacientes, y el 41% de los participantes en ensayos de cáncer, aunque representan el 51% de los pacientes.
Pero también se desvelaba que, más allá de las preocupaciones sobre la responsabilidad y los efectos secundarios, los conceptos culturales profundamente arraigados y los roles sociales dañan aún más la atención médica de las mujeres. Entre los hallazgos, se vio que las mujeres jóvenes participan más que las mayores, a pesar de que las enfermedades cardiovasculares aumentan de forma importante después de la menopausia. Además, las diferencias geográficas también resultaron muy relevantes, lo que apunta a la influencia de factores socioculturales en la participación de las mujeres.
Derribar barreras
El especialista pone ejemplos de paradojas que tienen lugar en las fases de investigación de medicamentos desarrollados para la insuficiencia cardiaca: “La población que habitualmente se incluye en estos ensayos es mayoritariamente masculina, de entre 63 y 67 años, pero el perfil de españoles con insuficiencia cardiaca que normalmente toma estos fármacos son predominantemente mujeres con edades superiores a los 75 años”. La realidad es que es complicado tener representación de personas de todos los niveles socioeconómicos, de diferentes orígenes, si viven en zonas rurales o urbanas…
Otras veces, las mujeres no acceden a los ensayos por falta de información o miedo a las pruebas. Así lo desvela un trabajo realizado conjuntamente por la Fundación Pasqual Maragall y la fundación Women’s Brain Foundation y que ha sido publicado en la revista Alzheimer’s Research & Therapy. El estudio concluyó que es necesario adaptar nuevas estrategias de reclutamiento, ya que uno de los hallazgos más relevantes es que las mujeres solteras con mayor nivel educativo muestran una menor disposición a someterse a procedimientos invasivos como la punción lumbar. Son resultados interesantes, porque ponen de manifiesto la necesidad de integrar las necesidades específicas de las mujeres en la información que se ofrece sobre los ensayos clínicos, además de explorar alternativas menos invasivas, como los biomarcadores en sangre, que son moléculas –como proteínas, hormonas o genes– que se pueden medir a través de un análisis de sangre para detectar enfermedades o estudiar cómo está funcionando un tratamiento.

¿Qué queda por hacer?
“Aunque una de las razones clásicas para no incluir mujeres en los ensayos clínicos estaba dirigida a su protección, para evitar que en caso de embarazo se pudiera someter al feto a un tratamiento con riesgo para su desarrollo, en la actualidad hay medidas suficientes como para poder incluir con seguridad mujeres en ensayos clínicos”, explica Borobia. Y, poco a poco, se desarrollan nuevas estrategias que fomentan la inclusión de las mujeres en los ensayos clínicos.
En enero del 2025, y en relación al interés conjunto que existe por una investigación más inclusiva, la FDA emitió una guía dirigida a la industria biomédica con tres puntos clave para poner en marcha:
- Inclusión total de las mujeres en los ensayos clínicos, con recomendaciones específicas para que participen incluso en ensayos de fase 1 y fases tempranas de fase 2, que son en las que se determina la seguridad de un fármaco o tratamiento. En lugar de excluirlas para evitar el riesgo de embarazo durante el ensayo, la FDA solicita a los investigadores monitorear los embarazos para garantizar la seguridad del estudio.
- Recoger datos relacionados con el sexo y analizarlos junto con otras variables como edad o raza. Esto significa que los investigadores deben incluir una representación justa de ambos sexos para detectar diferencias significativas en la respuesta a los medicamentos.
- Evaluar tres efectos de los fármacos durante el ensayo. Efectos en el ciclo menstrual, efectos de terapias hormonales exógenas que consisten en administrar hormonas de una fuente externa, y efectos del medicamento sobre los anticonceptivos orales.
En definitiva, la infrarrepresentación de las mujeres en los ensayos clínicos no es solo una cuestión histórica, sino un problema que sigue condicionando los diagnósticos, la eficacia de los tratamientos y la seguridad de los medicamentos. Avanzar hacia una investigación más inclusiva, que tenga en cuenta el sexo, la edad y el contexto social, no solo permite mejorar la atención a las mujeres, sino que es un paso imprescindible para construir una medicina más eficaz, más segura y verdaderamente personalizada para toda la población.